Servizi AR Svizzera
Rappresentante autorizzato svizzero per i dispositivi medici
e la diagnostica in vitro


Sei passi per CH-REP
Grazie ai nostri processi semplificati ,possiamo registrare
i vostri prodotti in soli sei passi!

la giungla delle leggi
La sfida
Guardate il nostro breve video per saperne di più sull'argomento.

Professionale
La vostra soluzione
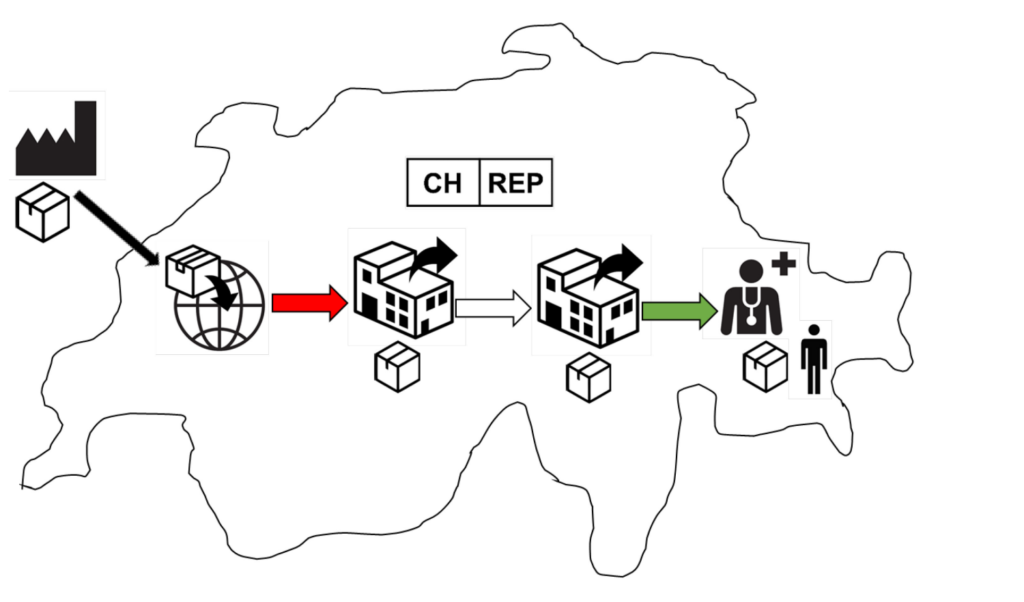
Swiss AR Services AG offre il servizio di rappresentante autorizzato svizzero per i dispositivi medici e la diagnostica in vitro. Grazie ai nostri contratti e ai processi appositamente adattati ai requisiti CH-REP, possiamo effettuare il nostro onboarding con voi in modo rapido e semplice e quindi agire come rappresentante svizzero per i vostri prodotti.
Contattateci oggi stesso
Rappresentante autorizzato svizzero

Core business
Vita quotidiana
Lo Swiss AR Issue Tracker fornisce un modo semplice per comunicare e tenere traccia dei reclami dei clienti, delle attività commerciali o di altre azioni rilevanti tra il produttore legale e Swiss AR Services AG in qualità di rappresentante autorizzato.
MDR / IVDR
Regolamento


personale e aziendale
Protezione dei dati
Utilizzando il nostro Swiss AR Issue Tracker appositamente configurato, gestiamo i documenti sui nostri server e beneficiamo anche di un modo semplice per comunicare, tenere traccia dei reclami dei clienti, delle attività commerciali o di altre azioni rilevanti tra il produttore legale e Swiss AR Services AG come rappresentante autorizzato.

Professionale
Processi snelli
Per poter reagire in modo più rapido, flessibile ed efficiente alle esigenze del mercato e dei clienti, i nostri processi sono sempre ottimizzati in base alla lean administration. Il processo generale di onboarding si articola in sei fasi distinte.

Il nostro servizio
La chiave del mercato svizzero!
Grazie all'alto livello di soddisfazione del cliente, alle competenze necessarie e ai nostri processi snelli, vi accompagniamo come rappresentanti svizzeri direttamente a destinazione.
Avete domande?
FAQ
Siamo a vostra disposizione 5 giorni su 7 e vi risponderemo il più rapidamente possibile. In allegato troverete le risposte alle domande più frequenti delle nostre FAQ.
Contattateci oggi stesso tramite il nostro modulo di contatto.
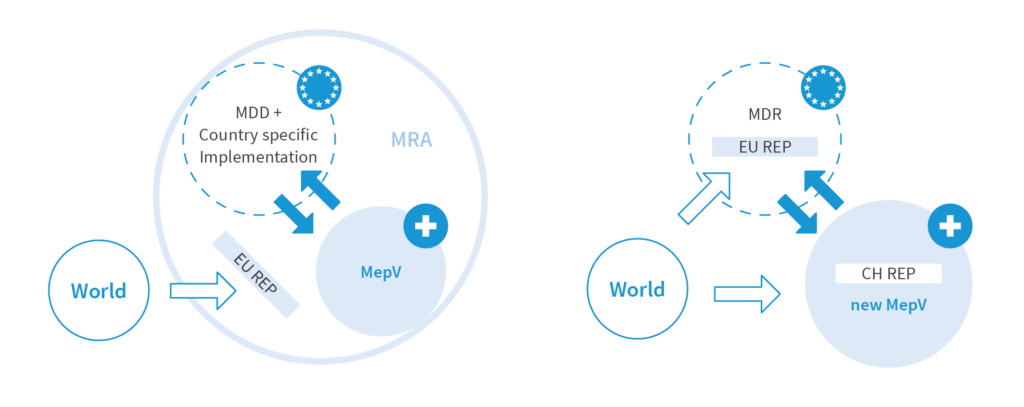
A causa del fallimento dei negoziati per un nuovo accordo quadro tra l'UE e la Svizzera, la valutazione della conformità dei dispositivi medici non è più riconosciuta reciprocamente dall'entrata in vigore della MDR (26.05.2021).
Dal 31 luglio 2022, tutti i prodotti MDD/MDR e le unità di trattamento di Classe I, II e III devono essere registrati per poter continuare a commercializzare dispositivi medici in Svizzera.
Le seguenti scadenze si applicano ai prodotti diagnostici in vitro:
(IVDD/IVDR)
- Fino al 31 marzo 2023 - Classe D
- Fino al 31 marzo 2023 - Classi C e B
- Fino al 31 luglio 2023 - Classe A
No.
Controlliamo solo che la dichiarazione di conformità UE e la documentazione tecnica siano state redatte e che il produttore abbia eseguito una procedura di conformità corrispondente, se applicabile.
Saremo lieti di consigliarvi un contatto adatto a questo scopo. Contattateci tramite il modulo di contatto.
Offriamo il servizio CH-REP per i dispositivi medici e i prodotti IVD.
